
英语原文共 10 页,剩余内容已隐藏,支付完成后下载完整资料
由明胶和透明质酸交叉连接而成的具有缓慢降解性的可注入水凝胶
摘要
我们开发了一种可注射的明胶/透明质酸水凝胶,具有缓慢降解性,由酰肼修饰的明胶(Gel-CDH)和透明质酸单醛(HA-mCHO)组成。明胶/透明质酸单醛水凝胶在磷酸盐缓冲溶液中的降解速度要比其他席夫碱交联明胶/透明质酸水凝胶慢得多,这些水凝胶由天然明胶、二酰肼修饰明胶或透明质酸二醛组成,因为稳定的席夫碱在醛和酰肼基团之间的形成,同时单醛改性抑制开环氧化。这种长时间的降解将适合于诱导血管生成。 因此,明胶/透明质酸单醛水凝胶在血管生成过程中具有足够的稳定性。此外,水凝胶的孔径为15minus;55mu;m,剪切储存模量为0.1minus;1kPa,适合支架应用。体外大鼠主动脉环试验显示明胶/透明质酸单醛水凝胶中微血管延伸的浓度依赖性。这些结果证明了明胶/透明质酸单醛水凝胶在组织工程支架中的潜在用途。
一.简介
原位交联水凝胶对于组织工程支架是有用的,因为它们可以被注射到模具中用于体外培养基质的制备,并被注射到组织缺陷中用于体内再生。支架适应移植部位后,实质细胞浸润支架,血管生成是必要的。为了实现有效的组织再生和机械稳定性,具有控制功能和性能的水凝胶支架是必不可少的。
细胞外基质(ECM)衍生聚合物被广泛用于水凝胶,因为它们可以提供与活组织相似的环境,适合血管生成和其他细胞募集。透明质酸(HA)和明胶(Gel)是这种ECM衍生聚合物的例子。 HA具有多种生物学功能,包括刺激细胞因子的产生和血管生成。凝胶,也是一种允许细胞附着的可生物降解、低免疫原聚合物的物质。由于HA和凝胶的这些功能,几种由凝胶和HA组成的可注射水凝胶已被开发用于组织工程支架。由硫醇化HA、硫醇化凝胶和聚乙二醇二丙烯酸酯组成的水凝胶支架,被开发用于管状组织结构,并作为修复骨软骨缺损的填料。 Cloyd等人在髓核载体的无侧限压缩中,将部分氧化的HA和有适当材料性能的凝胶混合制备水凝胶。Kageyama等人制备了可支持体外灌注血光网络的酰肼修饰凝胶和氧化HA基水凝胶。
为了利用这些基于ECM的可注射水凝胶作为支架,控制水凝胶的性能,包括降解动力学和机械强度是非常重要的。例如,理想的水凝胶支架应该以最佳的速率降解,逐渐被再生组织取代,最终从体内排出。这种最佳降解率将取决于各种因素,包括组织类型和大小。例如,在大鼠中,神经髓鞘化需要大约2minus;8周,然而脱细胞膀胱基质需要12周的时间来恢复与正常膀胱相当数量的平滑肌。此外,受体肝体积在活的右瓣移植后1minus;2个月翻了一倍。因此,需要一种在几周至几个月内控制可注射水凝胶支架降解动力学的方法。
为了控制降解速率,研究了各种化学交联方法,包括Michael加成,点击反应,席夫碱基形成。其中,席夫碱基形成由于快速交联和良好的生物相容性而得到了广泛的探索。 它已被用于制备各种聚合物的水凝胶,包括凝胶/羧基甲基纤维素、壳聚糖/HA、凝胶/海藻酸钠。尽管有许多以前的研究,控制降解率仍然是希夫的基础交联水凝胶的一个挑战。最近的研究表明,席夫碱的水解稳定性通过降低碳基的亲电性得到了增强。CN双键和pi;minus;pi;共轭有助于水解稳定性,向此共轭电子捐赠增加了胺衍生物的亲核性。当以羟胺和酰肼为对应物时,在生理pH下稳定水解的肼或氧杂交联水凝胶以苯甲醛为羰基。为了控制可注射水凝胶的降解速率,交联结构的影响需要进一步研究。
在本研究中,我们合成了一种新的凝胶衍生物,酰肼(CDH)改性凝胶。由于CDH形成的亚胺结构产生共振结构,CDH修饰的凝胶比天然凝胶有助于更稳定的席夫碱形成。作为对应物,采用单醛改性HA侧链。单醛HA将有助于形成更稳定抗水解的水凝胶,而不是像含常规二醛HA的水凝胶简单地被碘酸盐氧化,因为据报道多糖的开环结构容易水解。采用天然凝胶和凝胶衍生物以及醛改性HA进行比较,研究了交联结构对凝胶/HA水凝胶稳定性的影响。此外,我们还通过体外细胞存活试验和体外大鼠主动脉环试验检测了水凝胶作为支架的潜力。
二.材料和方法
材料。猪皮肤A型凝胶由Nitta Gelatin(日本大阪)捐赠。透明质酸由Denka(日本东京)提供。 从Wako Pure Chemical Industries,Ltd.(日本大阪)购买了ADH、CDH、NaCl、乙醇、甘氨酸、2,4,6-三硝基苯磺酸钠(TNBS)、分子量约为1、2、15minus;25的聚乙二醇(PEG)和300minus;500k Da(用作凝胶渗透色谱(GPC)标准)、高碘酸钠(NaIO4)、乙二醇、叔丁基碳酸(T-BC)和二甲基亚砜(DMSO)福尔马林溶液)。 HOBT是从东京化学工业(日本东京)获得的。WSCD购自多肽类药物研究所(日本大阪)。(plusmn;)1-乙基3-Amino-1,2-丙二醇,Triton-X100和BS1 Lectin-FITC来自Sigma-Aldrich(圣路易斯,U.S.A。)。 NaBH3CN是从MERCK购买的。 约分子量为8、15、10和500kDa(GPC标准)的葡聚糖是从额外合成的(Genay,法国)。井板(IWAKI3860minus;096)是从AGC技术玻璃(静冈,日本)获得的。人脐静脉内皮细胞(HUVEC,C2517A)和EGM-2子弹药盒(CC-3162)来自Lonza(Bazel,瑞士)。细胞计数试剂盒-8和DAPI(4rsquo;,6-二氨基-2-苯基吲哚)溶液是从Dojindo实验室(熊本,日本)购买的)。
酰肼-改性凝胶的合成。对于CDH改性凝胶(Gel-CDH)的制备,在500mL的茄型烧瓶中放入300mL纯水并溶入3g Gel,搅拌加入2.2g CDH。边搅拌边滴入0.46gWSCD在10mL的H2O中,然后0.45g HOBt溶于10mL的DMSO中。将溶液的pH调整为5,室温进行酰胺化反应过夜。该产品透析进入约0.3M NaCl溶液、25%(v/v)乙醇溶液和纯水中分别需要2、1和4天,使用6000minus;8000Da分子量的透析膜切断和冻干。采用相同的方法合成了ADH改性凝胶(Gel-ADH),用ADH代替CDH,并作为对照材料。(图1)
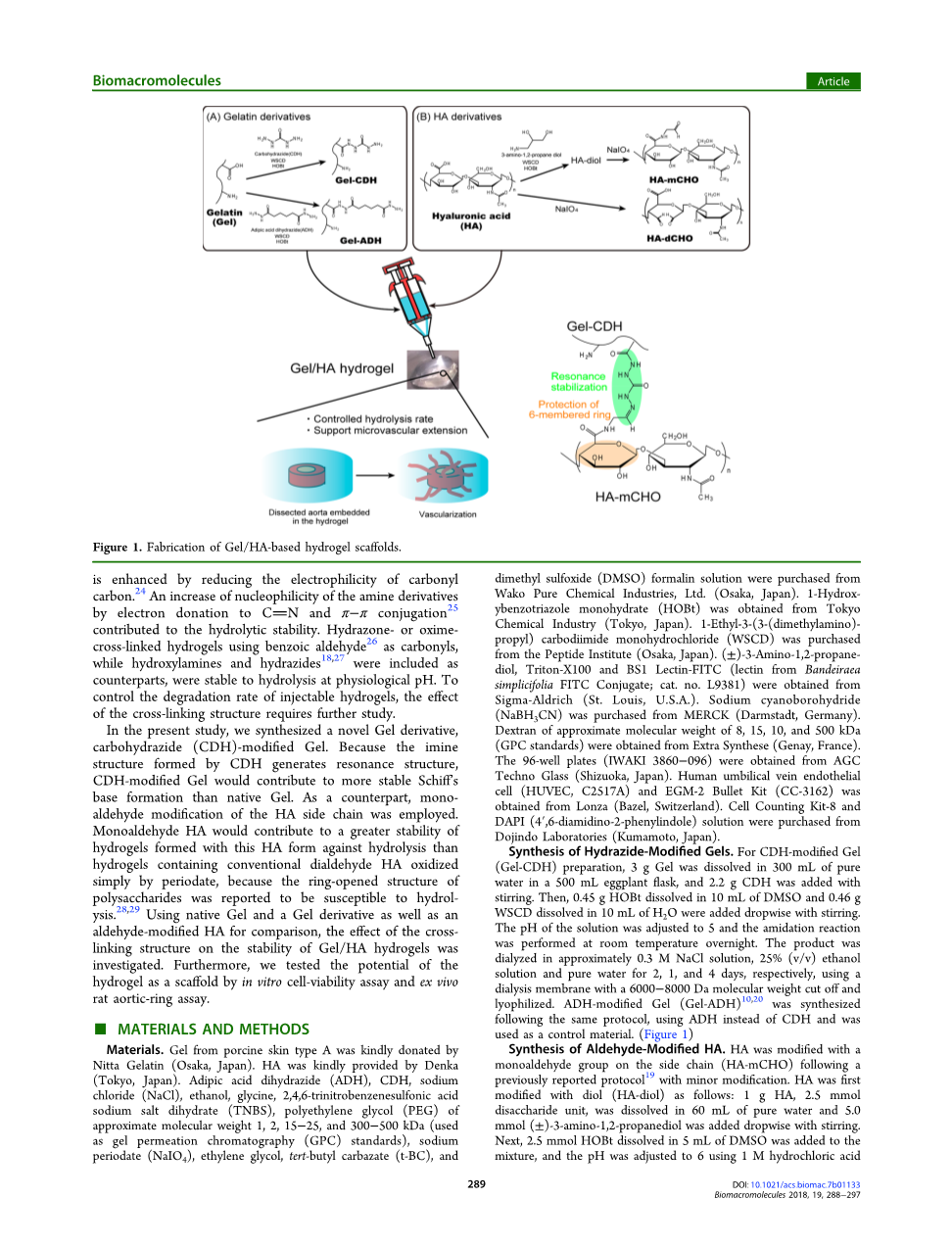
图1. 凝胶/基于HA的水凝胶支架的制造
醛修饰HA的合成。HA-mCHO是遵循先前报道的协议进行了轻微的修饰,在侧链上用单醛基团对HA进行了修饰。首先用二醇(HA-idol)对HA进行改性:1g HA,2.5mmol二糖单位溶于60mL的纯水中,搅拌滴加5.0mmol(plusmn;-3-氨基-1,2-丙二醇)。 接下来,将2.5mmol HOBt溶于5mL的DMSO中加入到混合物中,用1M盐酸将pH调节到6,然后将0.75mmol WSCD溶于5mL纯水中加入到混合物中。过夜反应后,用0.1M NaCl溶液和纯水分别透析2天和1天,用6000minus;8000Da分子量的透析膜切断和冻干。共轭二元醇基团被氧化得到HA-mCHO。共200mg HA-二醇溶于25mL的纯水中,滴加0.5mmol NaIO4溶于0.5mL的纯水中。在黑暗中搅拌进行氧化反应5分钟,然后加入10mmol乙二醇来猝灭反应。用6000minus;8000Da分子量的透析膜在纯水中透析1天,得到HA-mCHO。
在主链(HA-dCHO)上合成了醛改性的HA。 总之,200mg HA溶于25mL纯水中,0.5mmol NaIO4溶于0.5mL纯水中。 在黑暗中搅拌进行氧化反应1h,然后加入10mmol乙二醇。用6000minus;8000Da分子量的透析膜在纯水中透析1天,得到HA-dCHO。
通过与t-BC反应,再与NaBH3CN还原,确定醛基的改性比例。将醛改性的HA溶解在纯水中,浓度为10mg/mL和0.5MT-BC溶液中,比醛改性用的NaIO4过量10倍。混合物在室温下搅拌1h。 加入0.5M NaBH3CN水溶液,等摩尔至t-BC,并允许反应24h。样品在1000分子量的切断膜中透析纯化,冻干。 用alpha;JEOL JNM-LA400光谱仪(JEOL,东京,日本)对醛含量进行了1HNMR测量)。 通过比较叔丁基取代基(1.4ppm,9H)与HA乙酰胺(1.9ppm,3H)的信号,计算了醛的改性程度。
前驱体聚合物的表征。用配备岛津泵(LC-10AD)和折射率检测器(830-RI;Jasco,东京,日本)的TSK-GELGMPWXL测定合成前驱体聚合物的分子量。分别用PEG标准和右旋糖酐标准对照凝胶衍生物和HA衍生物。凝胶衍生物的流动相是0.2M磷酸盐缓冲液(pH 6.8),HA衍生物的流动相是加入0.2M NaCl(pH6.7)的50M磷酸盐缓冲液,流速为0.5mL/min。
此外,还测定了HA衍生物的降解动力学。将HA、HA-mCHO和HA-dCHO分别溶于50 mM磷酸盐缓冲液中,加入0.2M NaCl(pH 6.7),浓度为1mg/mL,在37℃保持8天。然后,用GPC测定HA衍生物的分子量。
用FT-IR分光度计(FT/IR-4200ST;Jasco,东京,日本)对凝胶和HA衍生物进行了傅里叶变换红外光谱(FT-IR),以确认改性。样品与溴化钾混合,形成片剂,测量在4000minus;400cm-1,分辨率为4cm-1。
凝胶/HA水凝胶的表征。在磷酸盐缓冲溶液(PBS)中制备了凝胶和HA衍生物溶液。水凝胶是用双筒注射器纤维蛋白胶水喷头(Baxter,Deerfield,U.S.A制备的。其中一个注射器装满凝胶衍生溶液,另一个注射器装满等量的HA衍生溶液。喷头装有18G针。我们制备了三种不同浓度的Gel/HA水凝胶:2.5%凝胶衍生物和1.0%HA衍生物、5.0%凝胶衍生物和2.0%HA衍生物、7.5%凝胶衍生物和3.0%HA衍生物。这些分别表示为低、中和高。参考前人的研究,测定了Gel-CDH/HA-mCHO水凝胶的凝胶化时间。
通过将0.4mL的水凝胶浸泡在PBS的20mL中,在37°C下,评估了水凝胶的溶胀和降解行为。水凝胶在不同的时间间隔内称重,直到样品完全降解。试验样品(Qt)的溶胀比定义为Qt=Wt/W0,其中Wt为溶胀水凝胶的重量,W0为水凝胶的初始重量。直到水凝胶被完全降解的时间被定义为降解的特征时间,当Qt=0时。
用扫描电子显微镜(SEM)在FE-SEMS-900(日立,东京,日本)上观察了水凝胶的形貌。水凝胶嵌入O.C.T混合冷冻在液氮中。用手术刀对样品进行切片,切片用铂涂层。水凝胶孔径是根据每个水凝胶的四个图像使用ImageJ软件决定(国立卫生研究院,贝塞斯达,U.S.A )。
进行动态粘弹性测量,以确定水凝胶的机械强度。线性粘弹性区域在5%应变下得到证实(数据未显示)。通过在不同浓度下混合等量的Gel-CDH和HA-mCHO溶液,制备直径为25毫米和高度为0.5毫米的水凝胶圆盘,然后在37°C下过夜孵育,以确保完全凝胶化。频率扫描试验在5%应变、37°C、10minus;0.01Hz进行,。
细胞活力测试。在Gel-CDH或HA-mCHO存在下,用细胞计数试剂盒8按照96孔板的标准方案测定体外细胞活力。在EGM-2子弹药盒中,HUVECs保持在37°C下,低于5%的CO2,并在第六段使用。 将HUVECs接种在4.8times;103细胞/井的96孔板上,用100mu;L培养基,在37°C下孵育5%CO2过夜。 100mu;L含有不同浓度Gel-CDH或HA-mCHO的EG
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[263430],资料为PDF文档或Word文档,PDF文档可免费转换为Word
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 可重写光存储器存储的光反应配位网络的可逆单晶一单晶转换外文翻译资料
- 蜘蛛网状氧化镍纳米线修饰的碳纳米线用于多层生物膜生长及其在高功率微生物燃料电池中的应用外文翻译资料
- TTF-CA的黑色多态性:TTF多态性和溶剂在机械化学和气相合成 、FT-IR、晶体包装和电子结构中的作用外文翻译资料
- 聚苯胺插层层状氧化钒纳米复合材料——一锅水热法合成及其在锂离子电池中的应用外文翻译资料
- 蚕茧衍生碳纤维的三维细胞粘附基质与吓啉铁组装, 用于监测细胞释放的信号分子外文翻译资料
- 用于催化的高嫡材料:一个新的前沿外文翻译资料
- 分子组装石墨烯与原子位点超快速实时检测一氧化氮细胞分析外文翻译资料
- 铋酸铜材料的光电化学分解水综合探究外文翻译资料
- 电催化硝酸盐减少对可持续氨生产发展的影响外文翻译资料
- 导电聚合物I贵金属纳米复合修饰电极的制备及其在 黄酒标龄鉴定中的应用外文翻译资料


