
英语原文共 6 页,剩余内容已隐藏,支付完成后下载完整资料
PH和外来离子对无定形石墨制备的氧化石墨烯吸附亚甲基蓝的影响
摘要
本文研究了用经济可行且资源丰富的无定形石墨(AG)制备的氧化石墨烯(GO)对亚甲基蓝(MB)的吸附。以及pH、外来离子和KClO4浓度对吸附MB的影响。通过XRD,FT-IR,XPS,AFM和分析仪来表征所制备的GO。结果表明:GO碳与氧的质量比(C / O)达到1.84,薄层(厚度小于2nm)占83.76%。分批实验的结果表明:在下列阳离子存在的情况下下对MB的吸附量逐渐减少有如下规律Li asymp;Na >K ,而在阴离子存在下则以ClO4minus;>NO3minus;>Clminus;的顺序减少。在含有ClO4minus;的溶液中吸附MB与溶液pH无关,这可能由于GO和ClO4minus;之间的协同效应。吸附过程由准二级动力学模型很好地描述,等温吸附模型与Langmuir等温吸附模型很好地吻合。
关键字:无定形石墨 无机离子 氧化石墨烯 亚甲基蓝 吸附率
1.前言
氧化石墨烯是石墨烯的氧化形式[1],有一系列的活性含氧官能团包括平面中的环氧化物、羟基以及在边缘的羰基和羧基[2,3]。通常,GO由鳞片石墨和合成石墨制备。AG是一种大量存在的天然石墨,晶体颗粒一般小于1mu;m ,结晶度较差[4],而且不经常用于合成GO。值得注意的是,因为其结晶度差,比表面积大,横向尺寸小[1,5],AG比鳞片石墨更容易氧化,GO表面上的含氧官能团(如-OH,-COOH)亲水性好而且负电荷密度大,这与污染物的去除又直接相关[6,7]。因此,AG应是用于合成GO吸附剂的潜在原料。
MB染料是一种对水质有害的杂芳族化合物,会导致各种环境问题[8]。与其他吸附剂相比包括印度叶[9],赤泥[10],甘蔗灰,锯屑[11],导电聚合物[12],活性炭[13]和碳纳米管[14] ,GO有巨大的比表面积,表面疏水性pi;-pi;相互作用,亲水,高负电荷密度且容易从大量天然石墨中获得[17,18],所以是最有希望的MB的吸附剂 [6,15,16]。此外,GO对MB染料的亲和力主要归功于GO上带负电的含氧官能团和MB分子上带正电荷的氨基之间的静电相互作用,而GO和MB染料分子的共轭芳香环局部pi;电子pi;-pi;相互作用可能也有助于吸附[15,17,19]。
外来离子对废水中污染物的吸附具有重要影响。Yang等人证实外来阳离子可以改变氧化多壁碳纳米管(MWCNT)的表面性质并影响对Ni(II)的吸附[20]。此外,Wang等人的报告称被吸附物与外来离子(Na 和K )之间对GO表面上活性位点的竞争可能影响其吸附能力[21]。Gao等人发现添加NaCl后GO对四环素的吸附能力降低[22]。而100mM Na 的存在可使GO对MB的吸附能力在其浓度为500mg / L时增加26%[15]。许多研究报道了外来离子对其他吸附剂吸附能力的影响[15,20-23]。然而,系统调查外来离子对GO吸附MB的影响仍然缺乏。
因此,本文研究了在各种外来离子(Li ,Na ,K ,Cl - ,NO3- 和ClO4-)存在下用GO吸附MB。 这项工作的目标是:(1)表征由无定形石墨制备的GO; (2)研究初始溶液pH,外来离子和KClO4-的浓度对GO吸附MB的影响;(3)研究GO对MB的吸附动力学和等温吸附模型。
2.实验
2.1.药剂
使用粒径为45~38mu;m纯度大于99%的AG来合成GO。使用的硫酸(98%)和盐酸(36%)来自信阳化学(中国)。所有其他分析级试剂购自国药化学试剂有限公司(中国)。去离子水(18.25M MOmega; cm)由Milli-Q Direct 16(Millipore Q,USA)生产。
2.2.氧化石墨(GrO)和GO的制备
使用Hummers方法[24]用AG制备GrO,如先前提到的[25,26]。将GrO粉末分散在去离子水(0.67mg / mL)中以形成黄棕色GrO悬浮液。然后,用Cole Parmer超声波处理器(750W和20kHz)以60%的振幅超声波剥离GrO悬浮液9分钟。最后,将胶体悬浮液在2520g下离心20分钟以除去未剥落的GrO,取含有GO的上清液。
2.3.测量方法
使用高级衍射仪(D8,Bruker,Germany)获得X射线衍射图案(XRD)。 通过傅立叶变换红外光谱仪(Vector-22,Bruker,Germany)检测傅立叶变换红外光谱(FT-IR)。在VG Multilab 2000光谱仪上测量X射线光电子能谱(XPS),并在284.6eV下用C1s线校正XPS光谱。用Vario EL立方分析仪(德国)对制备的GO粉末中碳,氧和氢的元素进行分析。使用具有测量峰值模式的Bruker MultiMode 8 AFM获得GO的原子力显微镜(AFM)图像。在25℃、NaCl浓度为5times;10 -3 mol / L的条件下,用配备有矩形电泳池的Malvern Zetasizer Nano ZS90(UK)进行GO的zeta;电位分析。
2.4MB吸附
使用分析级MB制备0.5g / L 的MB储备溶液。GO吸附MB的分批实验在锥形烧瓶中进行,向其中加入GO(0.6g / L),MB和外来离子(LiCl,NaCl,KCl,KNO3和KClO4)配置不同组分相对应的浓度。通过加入0.1mol / L HCl,HNO3,HClO4,KOH或NaOH溶液调节每个烧瓶中悬浮液的期望pH,添加体积可以忽略。通过机械振荡器(HZQ-C,Hangzhou Chincan Trading Co,Ltd,Hangzhou,China)以30rpm的搅拌速度,在规定的时间内将悬浮液摇匀。分离固相使用0.22mu;m膜从溶液中分离。通过UV分光光度计(Orion Aquamate 8000,Thermo,US)测定滤液中MB的浓度,在665nm的波长下使用以下方程计算MB吸附量:
(1)
其中C0和Ct(mg / L)分别是初始和终浓度下MB的液相浓度。V是溶液的体积(L),m是使用的吸附剂的质量(g)。使用以下方程计算吸附率:
(2)
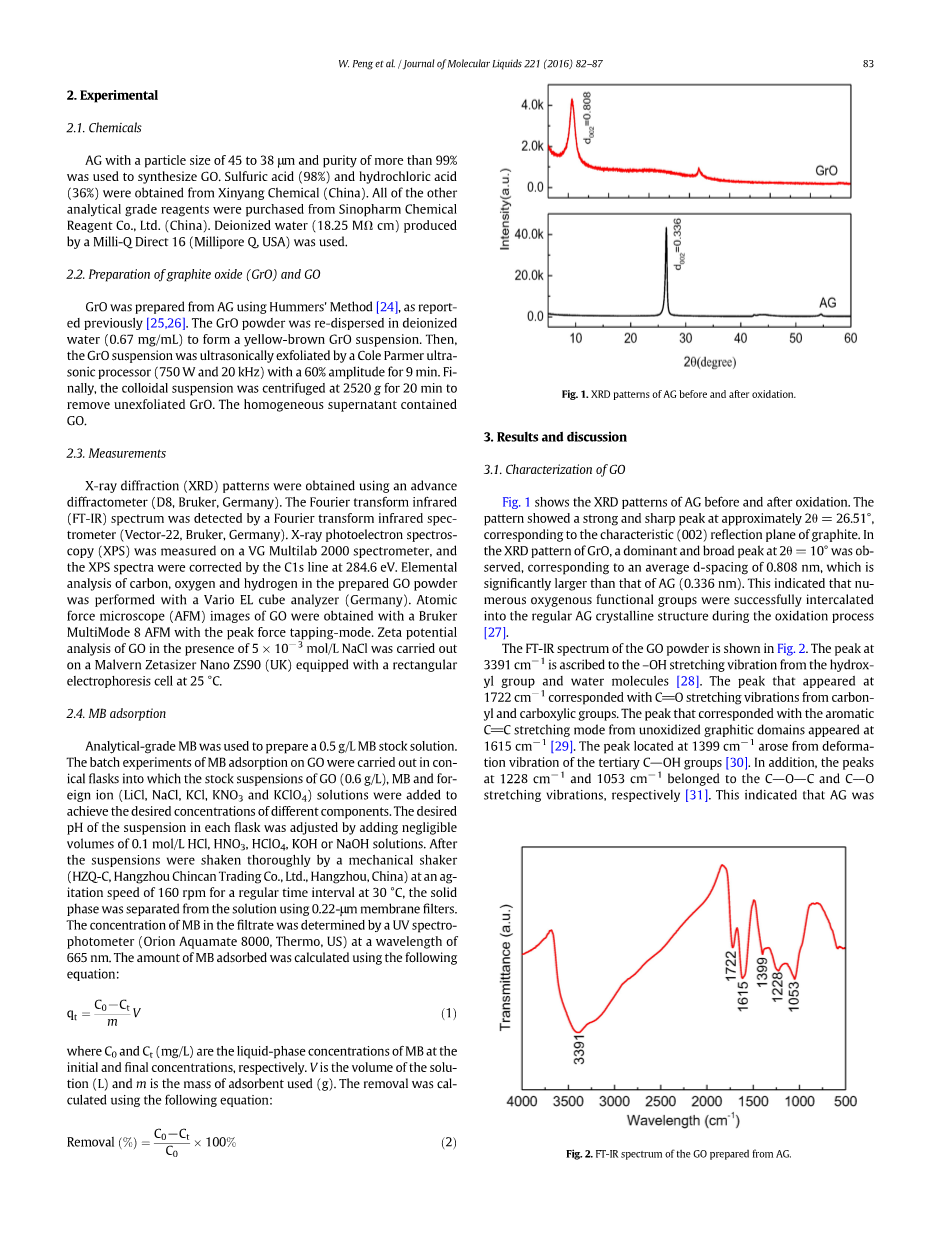
图1 AG氧化前后的XRD图谱
3.1.GO的表征
图1显示了AG氧化前后的XRD图谱。该图谱在约2theta;= 26.51°处显示强的尖锐峰,对应于石墨的特征反射面(002)。在GrO的XRD图中,观察到在2theta;= 10°处的主峰和宽峰,显著大于AG(0.336nm)的平均d间距0.808nm。这表明在氧化过程中许多含氧官能团被成功地插入常规AG晶体结构[27]。
GO粉末的FT-IR光谱如图2所示。 在3391cm-1处的峰是由于羟基和水分子的-OH伸缩振动[28]。在1722cm-1处出现的峰对应于来自羰基和羧基的C=O键的伸缩振动。在1615cm-1处的峰对应于芳香族与来自未氧化石墨的C=C键的拉伸[29]。在1399 cm-1的峰来自C-OH基团的变形振动[30]。此外,在1228cm -1和1053cm -1处的峰属于C-O-C键和C-O键的伸缩振动[31]。 这表明AG在氧化过程中被完全氧化,导致在GO片的表面上引入丰富的含氧官能团。
(透过率)
图2 GO粉末的FT-IR光谱
GO粉末的XPS测量光谱如图3a 所示。在GO中只观察到C1s和O1s峰位于284.6eV和531.0 eV处[32]。GO(图3b)的C1s XPS光谱为芳香环中C-C/C=C 键(284.6 eV)以及环氧基和烷氧基的C-O键 (286.4 eV),官能团C=O(288.3eV)和O –C=O(289.3eV)的四个峰[7,27,33],这与FT-IR光谱的结果不一致。
此外,测量所制备的GO粉末中的碳,氧和氢的相对含量分别为64.10%,34.77%和1.13%。碳和氧的质量比(C / O)达到1.84,表明在GO中存在大量含氧官能团。与用合成石墨制得的GO(C / O比率为2.3)和用的天然石墨制得的GO(C / O比率为2.0)相比,用AG制备的GO含有更多的含氧官能团,其被证明有利于从水溶液中吸附MB染料 [36]。
图4a为有代表性的GO 2D AFM图像。值得注意的是,图像中的大多数片层具有相似的颜色对比度,表明它们的厚度几乎相同。GO的典型厚度为约0.942nm,与常规制备的单一片层GO(0.7-1.2nm)相同[35,37,38]。 分析GO的400张2D AFM图像以确定片层厚度的分布。GO片层的厚度分布如图4c 所示。特别的,GO的厚度小于2nm(约1-2层)占83.76%。
图3用AG制备的GO横向扫描XPS光谱(a)和C1s峰 XPS光谱(b)。
图4 2D AFM形貌图(a),相应的厚度剖面图(b)和GO的厚度分布的直方图(c)。
3.2 吸附研究
3.2.1初始溶液pH的影响
初始溶液pH对GO的zeta;电位和对MB吸附率的影响如图5。在pH为2.0~12.0的范围内,GO的zeta;电位带负电,GO的对MB的去除效果明显地随初始溶液pH的增加而增加。当初始溶液pH从2.0增加到5.0时,负电荷值急剧增加,并且在5.0至12.0的pH范围内存在小的波动。
(吸附率)
)
图5初始溶液pH对GO和GO吸附的zeta;电位的影响
(初始条件:MB100mg / L,GO60mg / L)
GO的表面在pH 5.0~12.0的范围内带有负电荷,这可能归因于GO上的阴离子含氧官能团的去质子化[39]。高负电荷的GO薄片在溶液中的不仅能通过静电斥力均匀分散[40],还能增强与MB阳离子之间的吸引力,显着提高吸附效率[6,15,17]。此外,在吸附达到平衡后,通过去质子化从GO表面上的羧基释放更多的H 。释放的H 在pH更高溶液下的中和反应而耗尽,这将又有益于吸收[15]。
3.2.2外来离子的影响
图6显示了在0.01mol / L LiCl,NaCl,KCl,KNO 3或KClO 4存在下,不同pH条件下GO去除溶液中MB的情况。如图6a所示,在pH为2.0~12.0的范围内在KCl溶液中MB吸附率比在LiCl和NaCl溶液中更低,表明阳离子可以改变GO的表面性质并影响MB的吸附。GO对 MB的吸附可以认为是MB与外来阳离子(Li ,Na ,K )在GO表面竞争.K 的水合半径(2.32 Aring;)小于Na (2.76 Aring;)和Li (3.40Aring;)[41],因此K 对GO表面具有最高的亲和力,并且与GO表面上的含氧官能团进行反离子交换有最大倾向,这减少了GO表面上活性位点的数目。K 比Li 和Na 对MB吸附的影响更为明显。此外,外来阳离子可以降低MB与水的相互作用,使其更易接触GO [15]。根据外来离子对pH值较低时吸附Pb(II)的影响[20,42,43],在pH 为2.0~12.0下外来碱金属离子对MB吸附的影响大小是Li asymp;Na lt;K 。
图6外来离子对GO吸附MB的影响
(初始条件:MB 100 mg / L,GO 60mg / L,外来离子0.01mol / L)
离子浓度对GO吸附MB的影响
(初始条件:MB100mg / L,溶液pH 4.70)
另外,从图6b可以看出,外来阴离子严重影响MB去除。在KNO3和KClO4溶液中比在KCl溶液中对MB的去吸附率大,并且KClO4溶液中MB的吸附与初始溶液pH无关。这种现象可归因于:(1)根据无机酸根半径的顺序Cl-lt;NO3-lt;ClO4-[44],因为无机酸根半径较小的占有更多的离子交换位点,这导致GO吸附MB减少,这与在Cl-,NO3-和ClO4-存在下柠檬酸三铵-凹凸棒石表面对Ni2 的吸附一致[45]。(2)Cl-容易被GO表面上的相邻羟基或羧基
全文共12188字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[144810],资料为PDF文档或Word文档,PDF文档可免费转换为Word
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。


